Kỹ thuật chăn nuôi
TÍNH LƯỢNG KHOÁNG ĐỂ XỬ LÝ MẤT CÂN BẰNG ION Ở CÁC AO NUÔI TÔM ĐỘ MẶN THẤP
Cần xác định số lượng các cation chủ yếu để giải quyết thách thức về mất cân bằng ion trong các ao nuôi tôm có độ mặn thấp.
Nồng độ thấp của kali, đôi khi là của magiê có thể ảnh hưởng xấu đến tỷ lệ sống và tăng trưởng của tôm khi nước ao nuôi có độ mặn thấp.
Tuy nhiên, việc xác định số lượng muối cần thiết để chống lại sự mất cân bằng ion là một vấn đề, bởi vì nồng độ tối thiểu của cation chủ yếu (Na+, K+, Ca2+ và Mg2+) cần thiết cho các chức năng sinh lý của các loài thuộc họ tôm he hiện không được biết một cách chắc chắn. Do đó, việc lấy tỷ lệ nồng độ một số khoáng chính trong nước biển làm chuẩn để bổ sung là lựa chọn duy nhất hiện tại.
Nồng độ các ion trong nước có độ mặn thấp không chỉ đơn giản xuất phát từ sự pha loãng của nước biển. Các nồng độ này phụ thuộc vào kiểu, số lượng và tính chất hòa tan của các muối có trong đất, cấu tạo địa chất ở các nơi nước ao tiếp xúc cũng như tùy thuộc vào khí hậu. Tỷ lệ các cation chính trong nước mặn ở tầng mặt và nước ngầm có thể khác nhau hoàn toàn khi ở ngoài biển và vùng cửa sông.
Natri và kali đều mang một điện tích dương, và sự hấp thu kali của tôm có thể bị ảnh hưởng bởi nồng độ natri và ngược lại. Điều này cũng đúng khi áp dụng đối với magiê và canxi. Hơn nữa, tôm hấp thu các ion bằng mang của chúng trên cơ sở nồng độ mol (M) hơn là dựa vào khối lượng hay thể tích. Nồng độ mol của các cation chính được tính theo g/l chia theo khối lượng phân tử (natri: 32g; kali 29,1g; canxi: 40,08g; magiê: 24,31g). Tỷ lệ nồng độ mol của bốn ion trên trong nước biển xấp xỉ bằng 32,8:5,6:1,3:1,0.
TÍNH LƯỢNG KHOÁNG CẦN THIẾT
Cần xác định thành phần khoáng trong các sản phẩm thường dùng để bổ sung khoáng vào nước NTTS ( bảng 1)
Bảng 1: Tỷ lệ thành phần khoáng có trong các sản phẩm thường dùng để bổ sung khoáng vào nước NTTS:
| TÊN | CÔNG THỨC HOÁ HỌC | KHOÁNG CHẤT CHÍNH | % KHOÁNG CHÍNH | Tính tan trong nước |
| MAGNESIUM SULPHATE MONOHYDRATE | MgSO4.1H20 | Mg | 16% | Tan |
| MAGNESIUM SULPHATE PENTAHYDRATE | MgSO4.7H20 | Mg | 9,86% | Tan hoàn toàn |
| MAGNESIUM CLORUA HEXAHYDRATE | MgCl2.6H2O | Mg | 12% | Tan hoàn toàn |
|
SODIUM BICARBONATE | NaHCO3 | Na | 27,1% | Tan hoàn toàn |
|
DCP – Dicalcium Phosphat | CaHPO4.2H2O | Ca | 23% | Ít tan |
|
Kali Clorua (Potassium Chloride) | KCl | K | 50% | Tan hoàn toàn |
| Canxi clorua | CaCl2.2H2O | Ca | 27% | Tan hoàn toàn |
Bảng 2. Hệ số nhân theo độ mặn (ppt, ‰) để các cation có nồng độ tương tự nước biển.
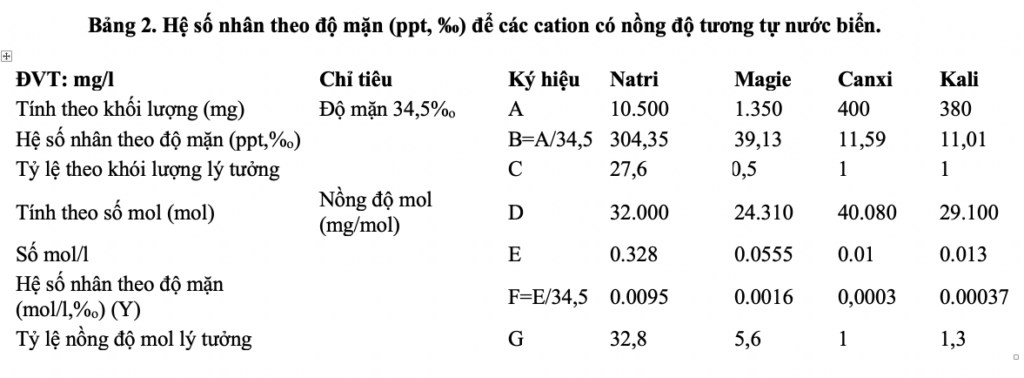
Ví dụ: Kiểm tra các chỉ tiêu khoáng trong ao nuôi tôm có thể tích 1.000 m3 = 1.000.000 lít (S) nước với độ mặn 8%0 bằng các thiết bị chuyên dụng ta có được được kết quả sau:
| ĐVT: mg/l | Nồng độ thực tế ( mg/l) | Nồng độ lý tưởng (mg/l) | Nồng độ cần bổ sung thêm (mg/l) |
| (a) | (b)= B*8 | (c)=(b)-(a) | |
| Magie | 225 | 313,04 | 88,04 |
| Canxi | 80 | 92,72 | 12,72 |
Cách 1: Tính bằng khối lượng gam ta có:
Nếu sử dụng MgSO4.1H2O hàm lượng Mg 16% (i) , Gọi số lượng khoáng MgSO4.1H2O cần sử dụng là M ta tính được như sau:
M= {(c) * S}/i = (88,04 * 1.000.000)/16% = 550.250.000 (mg) = 550 kg
Cách 2: Tính bằng số mol ta có:
| ĐVT: mg/l | Nồng độ thực tế ( mg/l) | Số mol (mol/l) | Nồng độ lý tưởng (mol/l) | Nồng độ cần bổ sung thêm (mol/l) |
| (a) | (a’)=(a)/D | (b’)= F*8 | (c’)=(b’)-(a’) | |
| Magie | 225 | 0,0093 | 0,0128 | 0,0035 |
| Canxi | 80 | 0,002 | 0,0024 | 0,0004 |
Nếu sử dụng MgSO4.1H2O hàm lượng Mg 16% (i) , Gọi số lượng khoáng MgSO4.1H2O cần sử dụng là M ta tính được như sau:
M= {(c’) * S*i = (0,0035*1.000.000)/16%= 21.875 mol => 21.875 *24.310 (mg/mol)= 531.781.250 mg = 531,8 kg.


